济南实验室李新钢教授、张迪研究员团队发表消化道迷走神经激活室旁核投射的孤束核GABA能神经元驱动睡眠的研究成果
济南微生态生物医学省实验室副主任李新钢教授及PI张迪研究员团队聚焦于“肠-脑轴”直接神经通路迷走神经调控中枢神经功能的环路机制问题,探究了该神经对睡眠的调控作用和中枢环路机制,并揭示了其在“食困“现象发生中的重要作用。2025年12月17日,该研究以“The gut vagal sensory pathway drives postprandial sleep via activation of PVH-projecting GABAergic neurons in the NTS”为题在《Nature Communications》发表。

本研究发现,当小鼠进食后,胃和十二指肠支配的迷走神经感觉神经元被激活,在向大脑发送“饱”的信号同时,通过独立环路,抑制动物清醒,引发”食困“。本研究从常见的”食困”现象出发,通过联合跨突触病毒示踪、单核RNA测序,光/化学遗传学操控等神经科学技术,发现了上消化道支配的迷走感觉神经元在调节睡眠-觉醒状态和促进餐后睡眠中的关键作用,并阐明了其驱动“食困”的神经环路机制。
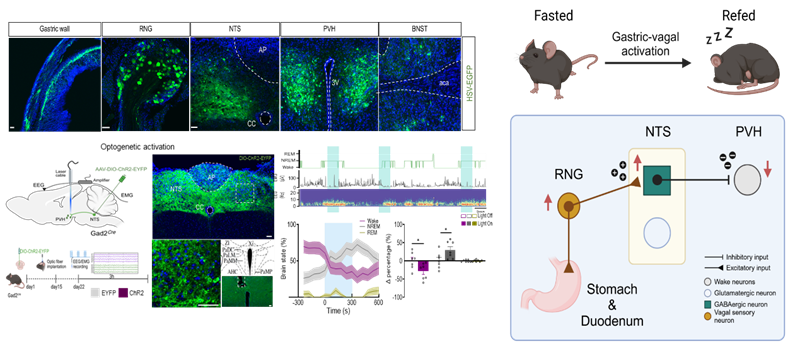
研究结果显示,摄食以及化学遗传学激活胃/十二指肠支配的迷走感觉神经元均可抑制小鼠的觉醒状态,并增加非快速眼动睡眠。相反,化学遗传学抑制则能消除摄食引起的“食困”现象。进一步研究发现,胃/十二指肠支配的迷走感觉神经元通过激活孤束核GABA能神经元来降低觉醒水平,环路解析显示,投射至下丘脑室旁核的孤束核GABA能神经元参与了迷走神经对睡眠-觉醒状态的调控。本研究明确了上消化道迷走感觉输入在睡眠-觉醒调控中的重要作用,鉴定了“胃/十二指肠→迷走结状神经节→孤束核GABA能神经元→下丘脑室旁核”这一上行通路,揭示了其在整合摄食行为与睡眠中扮演的关键角色。
科研启发:本研究从“肠-脑”最直接的神经通路-迷走神经感觉支出发,联合跨突触病毒示踪、单核RNA测序,光/化学遗传学操控等神经科学技术,发现了消化道迷走神经感觉支的激活对睡眠的促进作用,并解释了常见现象”食困” 背后的神经环路机制。本研究发现了一条具有普适性的睡眠调控神经环路,为睡眠障碍(如失眠、嗜睡症)以及代谢疾病引起的睡眠问题提供了全新的干预视角,对于这条神经通路的精准调控,有望为研发新的睡眠障碍治疗手段提供新策略。
李新钢教授和张迪研究员为论文共同通讯作者,研究生陈科华为论文第一作者。本项目得到国家自然科学基金资助项目(82071512)、山东省自然科学基金项目(ZR2019ZD33)和山东省实验室项目(SYS202202)的资助。