吴南屏教授、郑书发教授团队发表综述:Akkermansia muciniphila在炎症性肠病治疗中的免疫、代谢调控机制与进展
近期,济南微生态生物医学省实验室吴南屏教授与郑书发教授团队,聚焦炎症性肠病(IBD)的发病机制与治疗难题,系统剖析了肠道共生菌Akkermansia muciniphila的生物学特性,重点阐明了其通过调控肠道免疫与代谢网络改善IBD的核心机制,并深入探讨了该菌作为下一代益生菌的应用潜力与挑战。相关综述以“The role of Akkermansia muciniphila in the regulation of inflammatory bowel disease: intestinal immunity and metabolism”为题在《Frontiers in Immunology》发表。

炎症性肠病(IBD),包括克罗恩病(CD)和溃疡性结肠炎(UC),是一种慢性的肠道炎症性疾病,其发病与宿主免疫异常、肠道菌群失调及肠屏障功能受损密切相关。近年来,肠道菌群调控成为IBD治疗的研究热点,其中Akkermansia muciniphila 作为肠道黏液层的优势菌群,因具有黏液降解能力和潜在的益生特性,被认为是下一代益生菌的重要候选者。研究发现,IBD患者肠道中Akkermansia muciniphila丰度发生显著改变,且该菌的活菌、巴氏菌及其组分(外膜蛋白、胞外囊泡等)均展现出IBD保护作用。本综述从两大核心维度系统解析其在IBD中的作用机制:
1. 肠道免疫调控网络
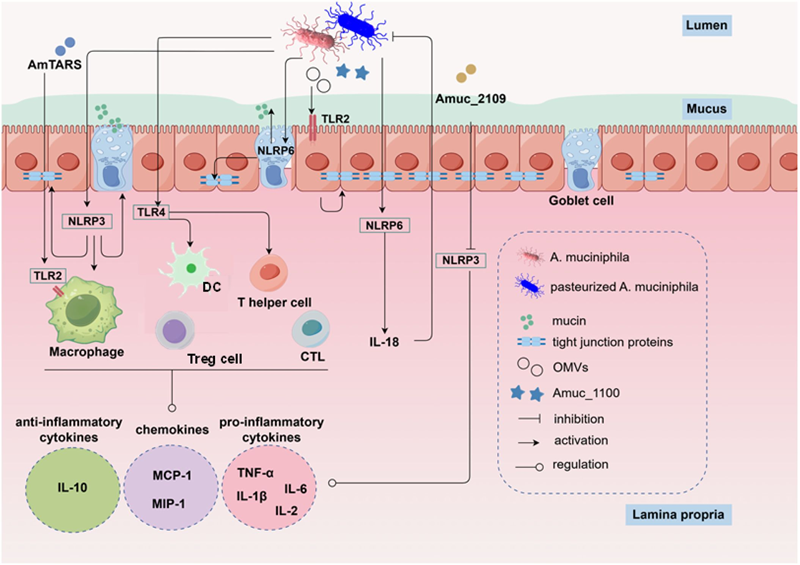
Akkermansia muciniphila通过与免疫细胞、肠道上皮细胞(IECs)及肠道干细胞(ISCs)的双向互作,重塑肠道免疫平衡:
· Akkermansia muciniphila的外膜蛋白Amuc_1100、分泌型苏氨酰-tRNA合成酶(AmTARS)、胞外囊泡(OMVs)等成分
(1)通过激活TLR2、TLR4信号通路,调控NLRP3、NLRP6炎症小体活性等途径,实现免疫细胞的调节,从而促进抗炎因子分泌,抑制促炎因子释放,减轻肠道炎症;
(2)促进肠道上皮紧密连接蛋白组装,刺激杯状细胞分泌黏液,修复黏液屏障损伤;
(3)通过激活Wnt/β-catenin等信号通路,促进ISCs增殖与肠上皮再生,强化肠道黏膜修复能力。
2. 肠道代谢调控通路
Akkermansia muciniphila 参与调控色氨酸(Trp)、短链脂肪酸(SCFAs)及胆汁酸(BAs)三大核心代谢通路的调控,协同改善IBD:
· (1)色氨酸代谢:通过抑制犬尿氨酸(Kyn)通路、激活吲哚-芳烃受体(AhR)通路,调节免疫应答与肠屏障功能。
· (2)SCFAs代谢:降解黏液产生乙酸、丙酸等SCFAs,进而激活GPR43受体促进Treg细胞分化等,抑制肠道炎症;
· (3)胆汁酸代谢:通过调节肠道菌群-胆汁酸轴,影响次级胆汁酸生成,激活FXR、TGR5等受体,维持肠屏障完整性并调控免疫反应。
科研启发:
该综述系统揭示了 Akkermansia muciniphila 调控IBD的免疫代谢双重机制,为理解肠道菌群与宿主互作提供了新视角。Akkermansia muciniphila及其组分凭借多靶点、协同性的抗炎特性,展现出巨大的IBD治疗潜力。然而,其作用仍存在争议,特定条件下可能加重炎症,且菌株特异性、定植规律及临床转化安全性等问题亟待解决。未来需进一步深入探究不同形式Akkermansia muciniphila的作用差异与分子机制,为开发精准靶向的微生物疗法提供理论支撑。
该研究得到济南微生态生物医学省实验室科研项目(JNL-2023012Q,JNL-2022005Q)、山东省自然科学基金(ZR2023QB299)、泰山学者奖励计划(tsqnz20230627)项目资助。