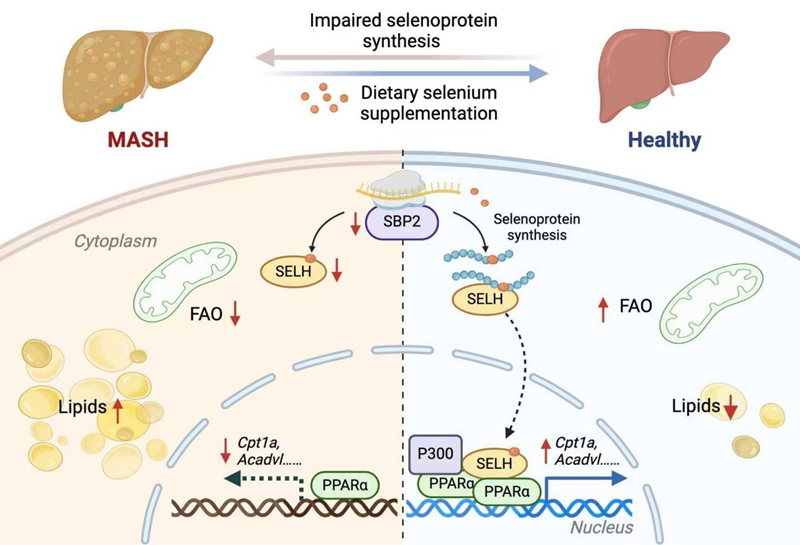
济南实验室顾晓松院士、江春平教授团队发现补硒通过SELENOH -PPARα轴促进肝脏的脂肪酸氧化
近日,济南实验室顾晓松院士、实验室副主任江春平教授团队联合中国科学院上海营养与健康研究所丁秋蓉教授团队,在代谢相关脂肪性肝炎(MASH)的研究中取得重要进展,首次揭示硒蛋白H(SELENOH)作为PPARα的协激活剂,将硒稳态与肝脂代谢连接起来,并预防脂肪性肝炎。该研究以“Selenoprotein H Functions as a PPARα Coactivator to Link Selenium Homeostasis to Hepatic Lipid Metabolism and Protect against Steatohepatitis”为题在《Advanced Science》(IF:15.6)上发表。

硒作为必需微量元素,主要通过25种人体硒蛋白发挥氧化还原调节等核心生物学功能,其缺乏与慢性肝病进展密切相关。MASH作为全球流行肝病,目前治疗手段有限。尽管研究表明硒状态显著影响肝脏脂质代谢——硒缺乏会导致脂代谢紊乱,而补硒在动物模型中可有效缓解肝脏脂肪堆积,但大多数硒蛋白的具体功能与作用机制仍不明确。
硒稳态与MASH的关联机制
研究发现,MASH患者和动物模型的肝脏中存在硒稳态失衡,表现为血清和肝脏硒水平降低、硒蛋白合成普遍受损。这一缺陷的关键原因在于硒蛋白生物合成的关键调控因子SECIS结合蛋白2(SBP2)的表达下降。补充硒或过表达SBP2均可恢复硒蛋白合成,有效缓解MASH病理进程。
硒蛋白H通过PPARα调控脂肪代谢
研究首次阐明SELENOH是硒发挥肝脏保护作用的关键效应蛋白。在MASH中,SELENOH表达下调。机制上,SELENOH并非发挥传统的氧化还原酶功能,而是作为转录辅助激活因子,与配体激活的PPARα结合,促进共激活因子P300的招募,从而驱动脂肪酸氧化相关基因表达,改善肝脏脂质代谢。SELENOH -PPARα轴是硒补充改善MASH的核心通路。
科研启发:
该研究首次揭示了硒缺乏通过SBP2介导的硒蛋白合成障碍加剧MASH进展,并创新性发现SELENOH作为PPARα的转录共激活因子,以非氧化还原方式调控脂肪酸氧化的分子机制,为理解微量元素代谢与核受体信号互作提供了全新范式。未来需进一步解析不同硒蛋白在肝脏微环境中的细胞特异性功能,并探索靶向该轴的安全有效干预策略。
本研究得到山东省重点研发计划(竞争性创新平台) (编号2025CXPT176)、济南微生态生物医学省实验室科研项目(编号JNL2025008B)和山东省泰山学者青年专家计划(编号tsqn202507393, 202408310)的资助。